豆科植物与根瘤菌的共生固氮是自然界氮循环的重要环节。经典的共生固氮起始于植物对根瘤菌表面的脂壳寡糖Nod Factor的识别。2007年,法国科学家Giraud等人报道了根瘤菌Bradyrhizobium sp. BTAi1与其宿主豆科植物Aeschynomene indica 的识别不依赖于Nod Factor,提示了一种新的未知固氮机制存在。随后,意大利化学家Molinaro等对根瘤菌Bradyrhizobium sp. BTAi1的脂多糖进行结构分析,发现其中的O-抗原是由一种全新结构的双环糖Bradyrhizose通过α-(1→7)糖苷键连接而成,并推测其可能在这种未知的固氮机制中扮演重要角色。
图1. 根瘤菌Bradyrhizobium sp. BTAi1在豆科植物田皂角Aeschynomene indica 中的共生成瘤
从细菌中难以分离得到足够量的该多聚糖以开展生物活性的研究。因此,需要依靠化学合成的手段来解决这一问题。化学合成可以提供一系列不同链长的寡糖,从而在三级结构上研究链长和构象对活性的影响。Bradyrhizose单糖是由半乳糖/肌醇反式并环而成的十碳糖,拥有8个羟基化的手性中心。俞飚(点击查看介绍)课题组以葡萄糖糖烯为原料,通过Ferrier II型重排等关键反应,以26步和9%的总收率完成了对Bradyrhizose单糖分子的首次合成。
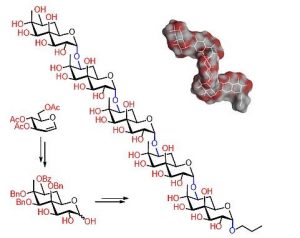
图2. 根瘤菌Bradyrhizobium sp. BTAi1中奇特结构O-抗原寡糖的结构和构象
接下来他们对Bradyrhizose单糖进行了克级制备,并仔细研究了其α-(1→7)糖苷化反应。Bradyrhizose分子的刚性结构、密集官能团和7位羟基的大位阻以及1,2-顺式糖苷键,给糖苷化带来了巨大的挑战。基于保护基对糖基底物电性的影响,他们利用给电子的苄基和吸电子的乙酰基来调控糖苷化底物的活性,再辅以乙酰基潜在的远程参与效应,成功抑制了Bradyrhizose糖苷化中诸多副反应的发生。最终,他们使用该课题组发展的广泛应用于三氟乙酰亚胺酯给体的方法,高立体选择性地制备了α-(1→7)连接的Bradyrhizose二糖、四糖和五糖。Molinaro等随之对这些寡糖的溶液构象进行分析,发现四糖和五糖都具备与天然多聚糖相似的右螺旋结构。这为进一步的固氮机制的研究打下了基础。
该研究成果已于近期发表在Angew. Chem. Int. Ed. 上。合成工作由俞飚课题组的李微博士完成。该研究工作得到了国家自然科学基金委和中科院等有关项目的资助。







